各區(qū)縣(自治縣)市場(chǎng)監(jiān)管局�����、衛(wèi)生健康委�����、醫(yī)保局�,重慶高新區(qū)市場(chǎng)監(jiān)管局����、公共服務(wù)局,萬(wàn)盛經(jīng)開(kāi)區(qū)市場(chǎng)監(jiān)管局���、衛(wèi)生健康局�����,市藥品監(jiān)測(cè)中心����,有關(guān)市級(jí)醫(yī)療衛(wèi)生單位:
?????? 為進(jìn)一步規(guī)范我市醫(yī)療機(jī)構(gòu)藥品不良反應(yīng)監(jiān)測(cè)與管理工作��,提升報(bào)告質(zhì)效和風(fēng)險(xiǎn)防控能力��,保障患者用藥安全����,結(jié)合我市實(shí)際����,制定了《重慶市醫(yī)療機(jī)構(gòu)藥品不良反應(yīng)監(jiān)測(cè)與管理工作指引》?����,F(xiàn)印發(fā)給你們,請(qǐng)相關(guān)醫(yī)療機(jī)構(gòu)參照改進(jìn)和提升藥品不良反應(yīng)監(jiān)測(cè)工作。
重慶市藥品監(jiān)督管理局
重慶市衛(wèi)生健康委員會(huì)
重慶市醫(yī)療保障局
2025年12月22日
重慶市醫(yī)療機(jī)構(gòu)藥品不良反應(yīng)監(jiān)測(cè)與管理工作指引9
??一���、總體原則
??(一)目的
??為進(jìn)一步規(guī)范重慶市醫(yī)療機(jī)構(gòu)藥品不良反應(yīng)監(jiān)測(cè)與管理工作,提升報(bào)告質(zhì)效和風(fēng)險(xiǎn)防控能力,保障患者用藥安全�,依據(jù)《藥品不良反應(yīng)報(bào)告和監(jiān)測(cè)與管理辦法》《藥物警戒質(zhì)量管理規(guī)范》等法律法規(guī)��,結(jié)合本市實(shí)際����,制定本工作指引����。
??(二)適用范圍
??本文件適用于指導(dǎo)和規(guī)范重慶市二級(jí)及以上醫(yī)療機(jī)構(gòu)藥品不良反應(yīng)監(jiān)測(cè)與管理工作開(kāi)展,其他醫(yī)療機(jī)構(gòu)可參照?qǐng)?zhí)行�����。
??(三)定義
??1.藥品不良反應(yīng)
??合格藥品在正常用法用量下出現(xiàn)的與用藥目的無(wú)關(guān)的有害反應(yīng)。
??2.嚴(yán)重藥品不良反應(yīng)
??因使用藥品引起以下?lián)p害情形之一的反應(yīng):導(dǎo)致死亡��;危及生命���;致癌�、致畸���、致出生缺陷�;導(dǎo)致顯著的或者永久的人體傷殘或者器官功能的損傷�;導(dǎo)致住院或者住院時(shí)間延長(zhǎng);導(dǎo)致其他重要醫(yī)學(xué)事件����,如不進(jìn)行治療可能出現(xiàn)上述所列情況的。
??3.新的藥品不良反應(yīng)(或非預(yù)期不良反應(yīng))
??藥品說(shuō)明書(shū)中未載明的不良反應(yīng)�。說(shuō)明書(shū)中已有描述,但不良反應(yīng)發(fā)生的性質(zhì)����、程度、后果或者頻率與說(shuō)明書(shū)描述不一致或者更嚴(yán)重的���,按照新的藥品不良反應(yīng)處理����。
??4.藥品群體不良事件
??同一藥品在使用過(guò)程中,在相對(duì)集中的時(shí)間��、區(qū)域內(nèi)��,對(duì)一定數(shù)量人群的身體健康或者生命安全造成損害或者威脅��,需要予以緊急處置的事件���。
??同一藥品:指同一生產(chǎn)企業(yè)生產(chǎn)的同一藥品名稱��、同一劑型�、 同一規(guī)格的藥品�。
??二、規(guī)范監(jiān)測(cè)與管理
??(一)完善監(jiān)測(cè)與管理工作體系
??1.設(shè)立藥品不良反應(yīng)監(jiān)測(cè)與管理工作組
??二級(jí)及以上醫(yī)療機(jī)構(gòu)設(shè)立藥品不良反應(yīng)監(jiān)測(cè)與管理工作組(以下簡(jiǎn)稱“工作組”)�����,組長(zhǎng)由主管醫(yī)療的分管領(lǐng)導(dǎo)擔(dān)任���,成員包括醫(yī)務(wù)、臨床科室���、藥學(xué)����、護(hù)理和質(zhì)量管理等部門負(fù)責(zé)人。工作組主要負(fù)責(zé)本機(jī)構(gòu)藥品不良反應(yīng)的統(tǒng)一管理與工作協(xié)調(diào)���,做好藥品不良反應(yīng)的信息收集�、分析�、評(píng)價(jià)、報(bào)告���、處置���、信息反饋、內(nèi)部審核和系統(tǒng)維護(hù)等工作���。
??2.設(shè)立藥品不良反應(yīng)監(jiān)測(cè)與管理辦公室
??工作組下設(shè)藥品不良反應(yīng)監(jiān)測(cè)與管理辦公室(以下簡(jiǎn)稱“辦公室”)�����。原則上����,辦公室設(shè)置在藥學(xué)部門,配備1名藥品不良反應(yīng)監(jiān)測(cè)與管理專(兼)職人員(以下簡(jiǎn)稱“管理員”)�����,負(fù)責(zé)藥品不良反應(yīng)報(bào)告的收集��、核實(shí)���、評(píng)價(jià)�、反饋及上報(bào)等具體工作���。管理員應(yīng)具有醫(yī)學(xué)藥學(xué)背景��,具備科學(xué)分析評(píng)價(jià)藥品不良反應(yīng)的專業(yè)技術(shù)能力����,專(兼)職時(shí)間不少于1年�����;崗位調(diào)整時(shí)���,做好工作交接��,并在國(guó)家藥品不良反應(yīng)監(jiān)測(cè)系統(tǒng)內(nèi)進(jìn)行個(gè)人信息更新���。
??3.設(shè)立藥品不良反應(yīng)監(jiān)測(cè)聯(lián)絡(luò)員
??醫(yī)療機(jī)構(gòu)臨床科室均內(nèi)設(shè)1-2名藥品不良反應(yīng)監(jiān)測(cè)聯(lián)絡(luò)員(以下簡(jiǎn)稱“聯(lián)絡(luò)員”),聯(lián)絡(luò)員由醫(yī)生和(或)護(hù)士擔(dān)任�����,負(fù)責(zé)本科室藥品不良反應(yīng)的收集���、核實(shí)�、上報(bào)等工作���。
??(二)明確監(jiān)測(cè)與管理重點(diǎn)任務(wù)
??1.藥品不良反應(yīng)監(jiān)測(cè)與管理工作組
??(1)制定本醫(yī)療機(jī)構(gòu)的藥品不良反應(yīng)監(jiān)測(cè)與管理工作制度�;
??(2)組織本醫(yī)療機(jī)構(gòu)藥品不良反應(yīng)宣傳教育和業(yè)務(wù)培訓(xùn)�;
??(3)制定及實(shí)施藥品不良反應(yīng)監(jiān)測(cè)與管理工作計(jì)劃和獎(jiǎng)懲措施;
??(4)按要求調(diào)查處置本機(jī)構(gòu)發(fā)生的藥品群體不良事件����;
??(5)組織開(kāi)展藥品不良反應(yīng)監(jiān)測(cè)質(zhì)量監(jiān)督和內(nèi)部審核工作。
??2.藥品不良反應(yīng)監(jiān)測(cè)與管理辦公室
??(1)開(kāi)展本機(jī)構(gòu)藥品不良反應(yīng)監(jiān)測(cè)�、評(píng)價(jià)��、反饋及上報(bào)工作�,每季度發(fā)布本機(jī)構(gòu)藥品不良反應(yīng)監(jiān)測(cè)情況���,實(shí)時(shí)發(fā)布疑似藥品不良反應(yīng)及其他與用藥有關(guān)的有害反應(yīng)信息及資訊���;
??(2)開(kāi)展本機(jī)構(gòu)藥品不良反應(yīng)監(jiān)測(cè)與管理的培訓(xùn)、宣傳和學(xué)術(shù)交流活動(dòng)��,鼓勵(lì)將醫(yī)療機(jī)構(gòu)管理人員����、醫(yī)師及護(hù)理人員等納入培訓(xùn)對(duì)象;
??(3)開(kāi)展嚴(yán)重藥品不良反應(yīng)的調(diào)查與評(píng)價(jià)����,對(duì)嚴(yán)重不良反應(yīng)發(fā)生頻率較高的藥品進(jìn)行重點(diǎn)監(jiān)測(cè)與分析;
??(4)開(kāi)展每年度藥品不良反應(yīng)監(jiān)測(cè)數(shù)據(jù)分析和總結(jié)���。
??3.藥品不良反應(yīng)監(jiān)測(cè)聯(lián)絡(luò)員
??(1)收集��、上報(bào)本科室藥品不良反應(yīng)�����;
??(2)配合管理員進(jìn)行藥品不良反應(yīng)信息核實(shí)����、事件分析���、信號(hào)識(shí)別�、風(fēng)險(xiǎn)處置等工作�;
??(3)對(duì)本科室患者進(jìn)行藥品不良反應(yīng)宣教等工作;
??(4)認(rèn)真執(zhí)行本機(jī)構(gòu)藥品不良反應(yīng)監(jiān)測(cè)與管理工作制度及標(biāo)準(zhǔn)操作規(guī)程�����。
??三���、加強(qiáng)藥品不良反應(yīng)處置
??醫(yī)療機(jī)構(gòu)獲知或發(fā)現(xiàn)藥品不良反應(yīng)時(shí)�,按照“監(jiān)測(cè)-報(bào)告-處置-反饋-檔案管理”的順序進(jìn)行處置�。
??(一)監(jiān)測(cè)
??1.監(jiān)測(cè)范圍
??患者使用藥品發(fā)生與用藥目的無(wú)關(guān)的有害反應(yīng),當(dāng)無(wú)法排除反應(yīng)與藥品存在相關(guān)性��,均應(yīng)按照“可疑即報(bào)”的原則報(bào)告�����。
??2.監(jiān)測(cè)重點(diǎn)
??醫(yī)療機(jī)構(gòu)應(yīng)重點(diǎn)收集新的和嚴(yán)重的不良反應(yīng)。醫(yī)療機(jī)構(gòu)根據(jù)藥品監(jiān)督管理部門的要求����,或根據(jù)本機(jī)構(gòu)藥品臨床使用和不良反應(yīng)監(jiān)測(cè)情況,對(duì)特定藥品開(kāi)展監(jiān)測(cè)���,如集采藥品����、創(chuàng)新藥���、特殊人群用藥等�����。
??(二)報(bào)告
??1.報(bào)告內(nèi)容
??醫(yī)療機(jī)構(gòu)獲知或發(fā)現(xiàn)藥品不良反應(yīng)后�,應(yīng)當(dāng)詳實(shí)記錄�、分析和處理,報(bào)告內(nèi)容參見(jiàn)《藥品不良反應(yīng)/事件報(bào)告表》(附件2)�,若發(fā)生群體不良事件還應(yīng)同時(shí)填寫《藥品群體不良事件基本信息表》(附件3)。
??2.報(bào)告時(shí)限
??醫(yī)療機(jī)構(gòu)發(fā)現(xiàn)或獲知新的�����、嚴(yán)重的藥品不良反應(yīng)應(yīng)當(dāng)在15日內(nèi)報(bào)告,其中死亡病例須立即報(bào)告����;其他藥品不良反應(yīng)應(yīng)當(dāng)在30日內(nèi)報(bào)告;群體不良事件立即報(bào)告�����。有隨訪信息的�����,應(yīng)當(dāng)及時(shí)報(bào)告����。
??3.報(bào)告途徑
??醫(yī)療機(jī)構(gòu)獲知或發(fā)現(xiàn)可能與用藥有關(guān)的不良反應(yīng)��,按時(shí)上報(bào)至國(guó)家藥品不良反應(yīng)監(jiān)測(cè)系統(tǒng)��。發(fā)生藥品群體不良事件��,立即通過(guò)電話或者傳真等方式報(bào)所在地的區(qū)縣級(jí)藥品監(jiān)督管理部門��、衛(wèi)生行政部門�����,必要時(shí)可越級(jí)報(bào)告。
??(三)處置
??1.臨床處置
??(1)出現(xiàn)疑似藥品不良反應(yīng)后�,醫(yī)務(wù)人員應(yīng)立即評(píng)估患者情況,判斷是否為藥品不良反應(yīng)���,以及藥品不良反應(yīng)類型����,確定處理方案并及時(shí)予以救治�����;
??(2)在醫(yī)療文書(shū)中詳細(xì)記錄發(fā)生不良反應(yīng)的臨床癥狀��、采取措施及轉(zhuǎn)歸情況�,并主動(dòng)向聯(lián)絡(luò)員提供相關(guān)信息和資料,由聯(lián)絡(luò)員對(duì)事件進(jìn)行調(diào)查���、分析和報(bào)告��。
??2.后續(xù)處置
??(1)管理員按照國(guó)家藥品不良反應(yīng)監(jiān)測(cè)機(jī)構(gòu)發(fā)布的藥品不良反應(yīng)關(guān)聯(lián)性分級(jí)評(píng)價(jià)標(biāo)準(zhǔn)�,對(duì)藥品與疑似不良反應(yīng)之間的關(guān)聯(lián)性進(jìn)行科學(xué)、客觀的評(píng)價(jià)����;
??(2)對(duì)藥品不良反應(yīng)引起的死亡病例或群體事件,管理員向相關(guān)醫(yī)務(wù)人員詳細(xì)了解病例的基本情況���、藥品使用情況��、不良反應(yīng)發(fā)生及診治情況等���,必要時(shí)組織專家共同討論,撰寫分析報(bào)告��,并報(bào)醫(yī)務(wù)部門備案��。對(duì)藥品群體不良事件�,在必要時(shí)可采取暫停藥品使用等緊急措施�����,并積極配合藥品監(jiān)督管理部門�����、衛(wèi)生健康主管部門和藥品不良反應(yīng)監(jiān)測(cè)機(jī)構(gòu)的調(diào)查。
??(四)反饋
??藥品不良反應(yīng)監(jiān)測(cè)與管理辦公室應(yīng)當(dāng)對(duì)收集的藥品不良反應(yīng)報(bào)告和監(jiān)測(cè)資料進(jìn)行統(tǒng)計(jì)和分析���,建立信息反饋機(jī)制���,通過(guò)內(nèi)部OA、工作站彈窗�����、上報(bào)平臺(tái)頁(yè)面查看信息等多種形式和途徑���,每季度向醫(yī)務(wù)人員反饋相關(guān)信息���,充分發(fā)揮警示提醒作用,形成不良反應(yīng)報(bào)告源于臨床��、服務(wù)于臨床的良性循環(huán)����。
??(五)檔案管理
??醫(yī)療機(jī)構(gòu)藥品不良反應(yīng)監(jiān)測(cè)與管理辦公室負(fù)責(zé)藥品不良反應(yīng)監(jiān)測(cè)檔案管理工作,規(guī)范管理藥品不良反應(yīng)監(jiān)測(cè)工作的記錄與數(shù)據(jù)��,妥善保存藥品不良反應(yīng)監(jiān)測(cè)工作檔案��。檔案記錄應(yīng)當(dāng)真實(shí)、準(zhǔn)確��、完整����、可追溯。
??四�、加強(qiáng)質(zhì)量監(jiān)督
??藥品不良反應(yīng)監(jiān)測(cè)質(zhì)量監(jiān)督工作,應(yīng)當(dāng)納入醫(yī)療機(jī)構(gòu)醫(yī)療質(zhì)量安全管理體系進(jìn)行統(tǒng)一管理���。
??(一)質(zhì)量控制
??1.定期開(kāi)展藥品不良反應(yīng)監(jiān)測(cè)與管理的內(nèi)部審核�。由醫(yī)務(wù)或質(zhì)量管理部門開(kāi)展內(nèi)部審核工作�,總結(jié)存在的問(wèn)題和不足。每年至少開(kāi)展1次相關(guān)工作的綜合評(píng)價(jià)����,評(píng)價(jià)指標(biāo)包括但不限于:藥品不良反應(yīng)報(bào)告上報(bào)率(如報(bào)告數(shù)/出院人次)����,監(jiān)測(cè)報(bào)告的真實(shí)性、完整性�、準(zhǔn)確性和及時(shí)性,處置建議的合理性���,醫(yī)護(hù)人員��、患者的滿意度等��。
??2.完善藥品不良反應(yīng)“非懲罰性”主動(dòng)報(bào)告機(jī)制���。已建立藥品不良反應(yīng)上報(bào)考核指標(biāo)的醫(yī)療機(jī)構(gòu)��,需定期評(píng)估指標(biāo)的科學(xué)性與適用性����,確保符合臨床工作實(shí)際��。
??(二)持續(xù)改進(jìn)
??1.管理員應(yīng)加強(qiáng)藥品不良反應(yīng)監(jiān)測(cè)工作相關(guān)的業(yè)務(wù)學(xué)習(xí)和培訓(xùn)���,提高自身專業(yè)技能和知識(shí)水平�����,提升服務(wù)質(zhì)量���。
??2.每年至少1次總結(jié)藥品不良反應(yīng)監(jiān)測(cè)工作中發(fā)現(xiàn)的問(wèn)題,采取整改措施��。
??3.每年至少1次定期分析監(jiān)測(cè)數(shù)據(jù),對(duì)不良反應(yīng)多�����、安全隱患突出的藥品進(jìn)行用藥目錄優(yōu)化���。
??4.醫(yī)療機(jī)構(gòu)加強(qiáng)信息化建設(shè)�����,不斷優(yōu)化藥品不良反應(yīng)上報(bào)流程和方式���,提升上報(bào)便捷性。
??五��、強(qiáng)化組織保障實(shí)施
??(一)強(qiáng)化監(jiān)管聯(lián)動(dòng)����。切實(shí)加強(qiáng)“三醫(yī)”統(tǒng)籌協(xié)調(diào)和組織領(lǐng)導(dǎo),健全監(jiān)測(cè)評(píng)價(jià)制度���,形成“三醫(yī)”相互銜接、相互配合的全鏈條監(jiān)管格局��。
??(二)強(qiáng)化數(shù)據(jù)利用。藥品監(jiān)督管理部門�����、衛(wèi)生健康部門����、醫(yī)保部門加強(qiáng)溝通協(xié)調(diào),實(shí)現(xiàn)數(shù)據(jù)共享與反饋���、風(fēng)險(xiǎn)預(yù)警與識(shí)別等��,對(duì)已識(shí)別風(fēng)險(xiǎn)的藥品及時(shí)采取風(fēng)險(xiǎn)控制措施�����,形成不良反應(yīng)報(bào)告源于臨床���、服務(wù)臨床的良性循環(huán)。
??(三)強(qiáng)化培訓(xùn)指導(dǎo)�。著力建設(shè)監(jiān)測(cè)評(píng)價(jià)人才隊(duì)伍,加強(qiáng)人員培養(yǎng)和培訓(xùn)指導(dǎo)�,提高藥品不良反應(yīng)監(jiān)測(cè)評(píng)價(jià)人員信息收集、風(fēng)險(xiǎn)識(shí)別以及綜合分析評(píng)價(jià)等能力�����,促進(jìn)信息填報(bào)完整、內(nèi)容準(zhǔn)確規(guī)范��。
?????? 附件1
藥品不良反應(yīng)監(jiān)測(cè)工作流程圖
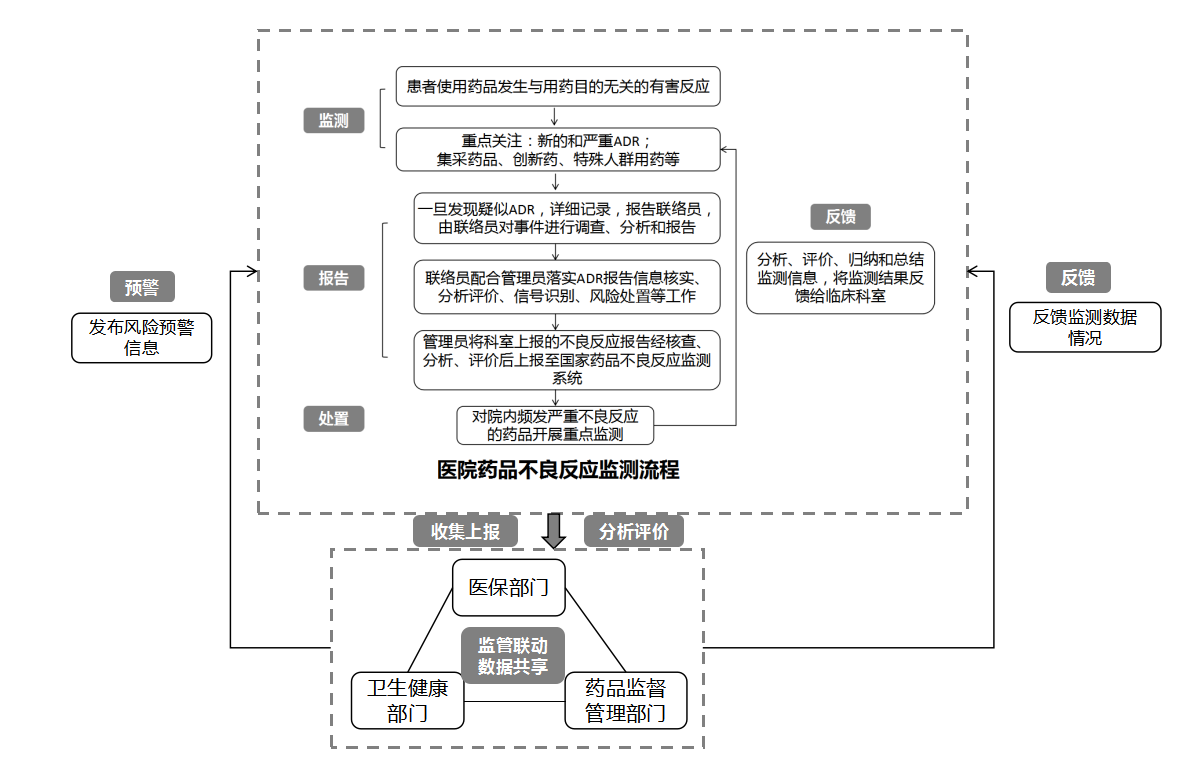
?????? 附件2
藥品不良反應(yīng)/事件報(bào)告表
首次報(bào)告□ ???????跟蹤報(bào)告□ ?????????????????????????????編碼:
報(bào)告類型:新的□ ?嚴(yán)重□ ?一般□ 報(bào)告單位類別:醫(yī)療機(jī)構(gòu)□ 經(jīng)營(yíng)企業(yè)□
生產(chǎn)企業(yè)□ ??個(gè)人□ ??其他□
|
患者姓名:
|
性別:男□女□
|
出生日期:年月日
或年齡:
|
民族:
|
體重(kg):
|
聯(lián)系方式:
|
|
原患疾?���。?
|
醫(yī)院名稱:
病歷號(hào)/門診號(hào):
|
既往藥品不良反應(yīng)/事件:有□無(wú)□不詳□
家族藥品不良反應(yīng)/事件:有□無(wú)□ 不詳□
|
|
相關(guān)重要信息: 吸煙史□ ?飲酒史□ ?妊娠期□ ?肝病史□ ?腎病史□ ?過(guò)敏史□其他□
|
|
|
藥品
|
批準(zhǔn)
文號(hào)
|
商品
名稱
|
通用名稱
(含劑型)
|
生產(chǎn)廠家
|
生產(chǎn)批號(hào)
|
用法用量
(次劑量、途徑��、日次數(shù))
|
用藥起止時(shí)間
|
用藥原因
|
|
|
懷疑藥品
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
并用藥
品
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
不良反應(yīng)/事件名稱:
|
不良反應(yīng)/事件發(fā)生時(shí)間:??年月日
|
|
|
不良反應(yīng)/事件過(guò)程描述(包括癥狀��、體征�、臨床檢驗(yàn)等)及處理情況(可附頁(yè)):
|
|
|
不良反應(yīng)/事件的結(jié)果:痊愈□ ?????好轉(zhuǎn)□ ?????未好轉(zhuǎn)□ ?????不詳□ ?????有后遺癥□ ?表現(xiàn):
死亡□直接死因:死亡時(shí)間:年 ???月 ???日
|
|
|
停藥或減量后,反應(yīng)/事件是否消失或減輕����?是□否□不明□未停藥或未減量□
再次使用可疑藥品后是否再次出現(xiàn)同樣反應(yīng)/事件?是□否□不明□未再使用□
|
|
|
對(duì)原患疾病的影響: 不明顯□ ??病程延長(zhǎng)□ ??病情加重□ ??導(dǎo)致后遺癥□ ??導(dǎo)致死亡□
|
|
|
關(guān)聯(lián)性評(píng)價(jià)
|
報(bào)告人評(píng)價(jià):??肯定□很可能□可能□可能無(wú)關(guān)□待評(píng)價(jià)□無(wú)法評(píng)價(jià)□簽名:?
報(bào)告單位評(píng)價(jià):?肯定□很可能□可能□可能無(wú)關(guān)□待評(píng)價(jià)□無(wú)法評(píng)價(jià)□簽名:
|
|
|
報(bào)告人信息
|
聯(lián)系電話:
|
職業(yè):醫(yī)生□藥師□? 護(hù)士□ ???其他□
|
|
|
電子郵箱:
|
簽名:
|
|
|
報(bào)告單位信息
|
單位名稱:
|
聯(lián)系人:
|
電話:
|
報(bào)告日期: 年月日
|
|
|
生產(chǎn)企業(yè)請(qǐng)
填寫信息來(lái)源
|
醫(yī)療機(jī)構(gòu)□ ???經(jīng)營(yíng)企業(yè)□ ???個(gè)人□ ???文獻(xiàn)報(bào)道□ ???上市后研究□ ???其他□
|
|
|
備 ??????注
|
|
|
?????? 附件3
藥品群體不良事件基本信息表
|
發(fā)生地區(qū):
|
使用單位:
|
用藥人數(shù):
|
|
發(fā)生不良事件人數(shù):
|
嚴(yán)重不良事件人數(shù):
|
死亡人數(shù):
|
|
首例用藥日期: ????????年 ?????月 ????日
|
首例發(fā)生日期: ?????????年 ?????月 ????日
|
|
懷疑藥品
|
商品名
|
通用名
|
生產(chǎn)企業(yè)
|
藥品規(guī)格
|
生產(chǎn)批號(hào)
|
批準(zhǔn)文號(hào)
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
器械
|
產(chǎn)品名稱
|
生產(chǎn)企業(yè)
|
生產(chǎn)批號(hào)
|
注冊(cè)號(hào)
|
|
|
|
|
|
|
|
|
|
本欄所指器械是與懷疑藥品同時(shí)使用且可能與群體不良事件相關(guān)的注射器��、輸液器等醫(yī)療器械�。
|
|
不良事件表現(xiàn):
|
|
群體不良事件過(guò)程描述及處理情況(可附頁(yè)):
|
|
報(bào)告單位意見(jiàn)
|
|
|
報(bào)告人信息
|
電話: ?????????????????????????電子郵箱: ??????????????????????簽名:
|
|
報(bào)告單位信息
|
報(bào)告單位: ?????????????????????聯(lián)系人: ????????????????????????電話:
|
報(bào)告日期:????年??月??日